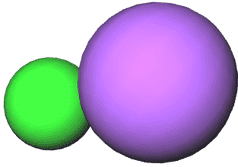
Vista 3D de la Molécula de NaCl (sal de mesa).
- Enlace Covalente: El enlace covalente es la fuerza que une dos átomos mediante la compartición de un electrón por átomo. Dentro de este tipo de enlace podemos encontrar dos tipos: el enlace covalente polar y el enlace covalente apolar. El primer sub-tipo corresponde a todos aquellos compuestos en donde la diferencia de electronegatividad de los átomos que lo componen va desde 0 hasta 1.7 (sin considerar el 0). Los compuestos que son polares se caracterizan por ser asimétricos, tener un momento dipolar (el momento dipolar es un factor que indica hacia donde se concentra la mayor densidad electrónica) distinto a 0, son solubles en agua y otros solventes polares, entre otras características. Dos ejemplos se ven en la Imagen EIE-3 (a) y en la Imagen EIE-3 (b), respectivamente. Por su parte, los compuestos que se forman por medio de enlaces covalentes apolares, no presentan momento dipolar, la diferencia de electronegatividad es igual a 0, son simétricos, son solubles en solventes apolares (como el hexano), entre otras cosas. La diferencia de electronegatividad cero se da cuando dos átomos iguales se unen entre sí, como por ejemplo la molécula de Nitrógeno o la molécula de Cloro (ver Imagen EIE-4 (a) e Imagen EIE-4 (b) respectivamente).
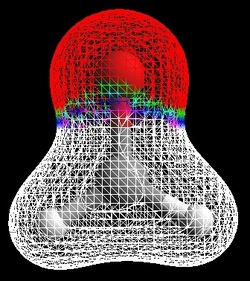
Imagen EIE-3: Densidades electrónicas en los siguientes compuestos polares: a) formaldehído (o metanal); b) 1,2-difluoretano. El color blanco indica una escasez de electrones, de ahí vienen respectivamente el color violeta, azul, verde y rojo (el cual indica mayor densidad electrónica).

No hay comentarios.:
Publicar un comentario